第2章 生命の起源
2.細胞の出現
全ての細胞についてその真の系統関係を復元し、いわゆる『生命の樹(系統樹)』を描けると仮定すると、ある「種」が別の「種」からどのように生じたかを推測し、その起源に至るまでの関係を追跡できる。それによって、最終的には地球上の全生命の共通祖先『最後の共通祖先(last universal common ancestor-LUCA)』が持っていた遺伝子構成が推定できる可能性がある。
しかし、「系統樹」という概念は、親から子への垂直遺伝を前提とした有性生殖に対して有効だが、細菌の場合は性を持たずに別の種を形成することがなく、さらに『遺伝子の水平移動』(注45)によって遺伝子をばらまき、少数の遺伝子を他の細菌へ渡すと同時に全ゲノムを自身の「娘(じょう)細胞」に伝達するという事実を考慮に入れると、「系統樹とは何か」、「系統樹から何を学べるのか」という根本的な問題が浮上する。
(注45)ある特定の生物が有する遺伝子または遺伝子群が,系統の異なる生物に組み込まれ機能すること。バクテリアでは、環境中に存在している遺伝子断片を取り込み、自身の染色体に組み込むことが知られている。また、真核生物にはウイルスを介した遺伝子の移動も知られている。これらの遺伝子移動は、生物の多様化や新規機能の獲得に重要な働きをしている。
進化生物学者ビル・マーティンは、この「系統樹」の問題点を認識しつつも、細菌の遺伝子系統樹に挑戦した。具体的な手法は別の文献を参照いただきたいが、彼は48の遺伝子を全生命から選び出し、それぞれについて遺伝子系統樹を作成し、50の『細菌』と50『古細菌』の関係を明らかにした。その結果、48の普遍的な遺伝子全てが、生命の系統樹で最も初期の分岐が細菌と古細菌の間であることを示した。つまり、
- 最後の共通祖先『LUCA』は、「細菌」と「古細菌」の共通祖先であった。
この結果を受けて、進化生化学者のニック・レーンたちは「LUCA」についての各種の可能性を詳細に検証した(詳細は、参考文献3を参照のこと)。その結果、
- LUCAは化学浸透共役(<物語り その3>注25)を利用し、ATP合成酵素を持っていたが、現代の膜や現代の細胞がプロトンを汲み上げるのに用いている巨大な呼吸鎖複合体は、持っていなかった可能性が残された。
さらに、
- LUCAはDNA、普遍的な遺伝コード、転写、翻訳、リボソームを有していたが、現代のDNA複製の手法は生み出していなかったことも明らかになった。
- この不思議な細胞は、開放的な海洋環境では生存が難しい一方で、前節で触れた「アルカリ熱水噴出孔」の環境を考え合わせると、その存在が可能であることが示唆される。重要な手がかりとなるのは、そのような熱水噴出孔で、細菌と古細菌がどのように生きているかという問いである。
- 少なくとも、これら生物の一部は、地球化学的な現象と類似性を持つ『アセチルCoA経路』という原始的に見えるプロセスによって生存していることが知られている。
そこで、この観察を検証してみよう。
現存する生物界全体において、炭素を固定、すなわち二酸化炭素などの無機分子を有機分子に変換するプロセスは、以下の6種類しかない。
- 還元的ペントースリン酸回路(カルビン回路):光合成生物のみに見られる
- 還元的アセチルCoA回路(ウッド・リュンガル回路):化学合成生物のみ
- 還元的クエン酸回路(逆TCA回路):光合成・化学合成生物ともに見られる
- ジカルボキシレート/4-ヒドロキシ酪酸(DC/4-HB)サイクル:化学合成生物のみ
- 3-ヒドロキシプロピオン酸/4-ヒドロキシ酪酸(3-HP/4-HB)サイクル:化学合成生物のみ
- 3-ヒドロキシプロピオン酸(3-HP)二重サイクル:光合成生物のみ
出典:フリー百科事典『ウィキペディア(Wikipedia)』「炭素固定」(https://ja.wikipedia.org/wiki/%E7%82%AD%E7%B4%A0%E5%9B%BA%E5%AE%9A)
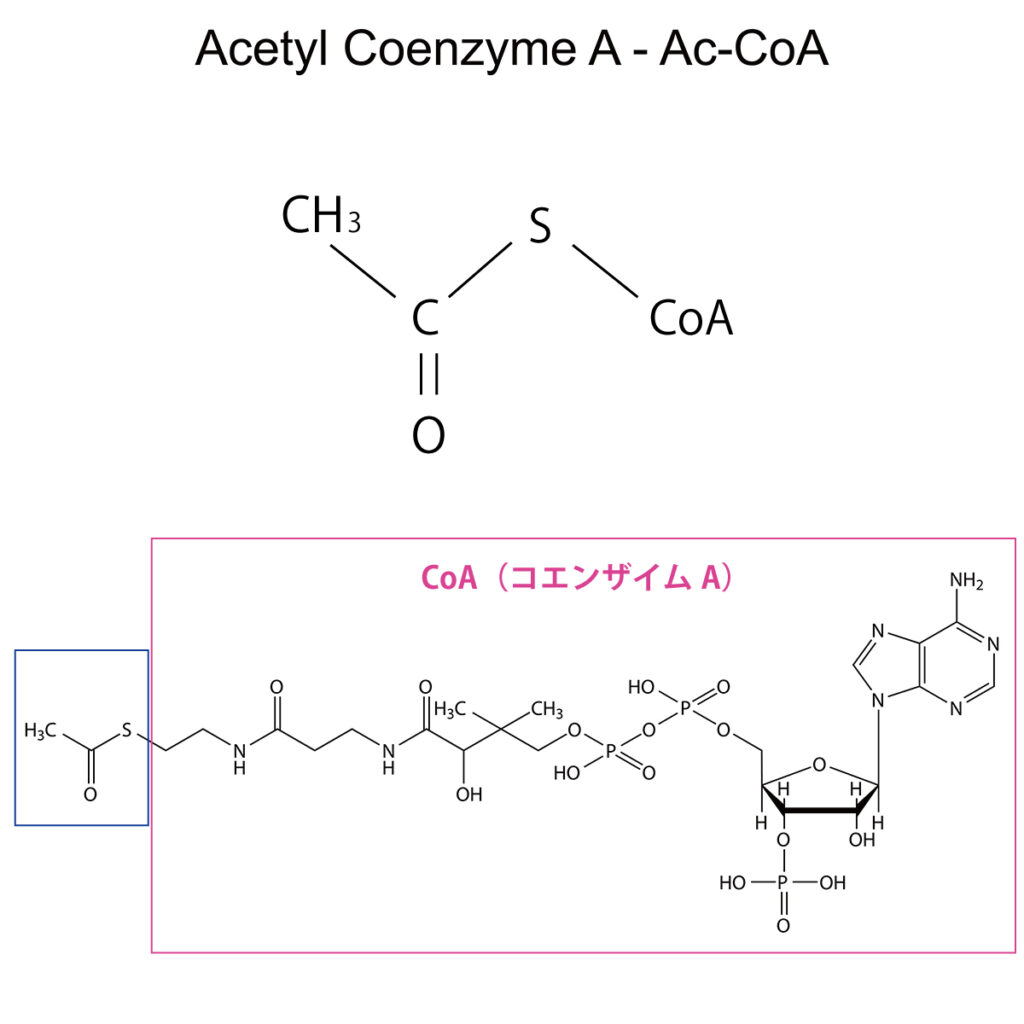
この6つの経路の中で、唯一、細菌と古細菌の両方に見られる炭素固定の経路が存在し、それは共通祖先であるLUCAに由来している可能性が高い。それが『アセチルCoA(注46)経路』である。
(注46)補酵素A (coenzyme A, CoA, C21H36N7O16P3S)と酢酸(CH3COOH)がチオエステル結合したもの(C23H38N7O17P3S , CH3CO-CoA)を『アセチルCoA』と呼び、『活性酢酸』とも称される。一部の酵素はタンパク質のみで活性を発現するが、活性発現には補酵素(コエンザイム、CoA)と呼ばれる低分子有機化合物が必要なものもある。さらに、『チオエステル結合』とは、カルボン酸とチオール(水素化された硫黄を末端に持つ有機化合物R-SH)が脱水縮合した構造 (R−CO−S−R’) を持つ化合物を指す。
「アセチルCoA経路」を利用する古細菌としては『メタン生成菌』、細菌では『酢酸生成菌』が存在する。アセチルCoA経路は、水素と二酸化炭素から始まる。これらは前節で触れた「アルカリ熱水噴出孔」において豊富に存在する分子である。そこで指摘したとおり、H2とCO2から有機物ができる反応は発エルゴン的、つまりエネルギーを放出する。理論上、その反応は自発的に起こるはずであるが、実際には、H2とCO2を速やかに反応できなくしているエネルギー障壁が存在する。メタン生成菌はプロトン勾配を用いてこの障壁を乗り越える。
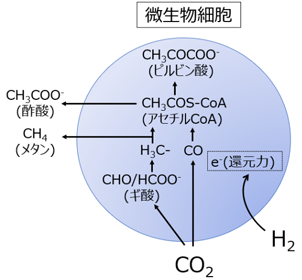
メタン生成菌も酢酸生成菌も、H2とCO2の反応だけで成長できる。これは、この反応が生育に必要な炭素とエネルギーをすべて供給するからである。この特性は、アセチルCoA経路が他の5つの炭素固定経路と異なる点である。
さらに、他の経路と異なり、アセチルCoA経路は直線的で短い。このことは、単純な無機分子をすべての細胞の代謝中心である反応性の高い小分子、「アセチルCoA」に変換する過程が少ないことを示している(図52)。「CoA(補酵素A)」は、酵素が小分子を処理できるようにするための普遍的な化学の『鉤(かぎ)』である。重要な部分は「かぎ」よりも「アセチル基」(CH3CO-)と呼ばれる吊されたものである。
補酵素Aに結合したアセチル基は、活性化状態(『活性酢酸』と呼ばれることも多く、要するに反応性の高い酢)であるため、ほかの有機分子と即座に反応可能であり、生合成(生体がその構成成分である生体分子を作り出すこと)を促進する。そのため、アセチルCoA経路は、H2とCO2から反応性の高い小有機分子を僅かなステップで生み出す。その過程で、ヌクレオチドなどの分子を形成させるだけでなく、それらを重合して長鎖化(DNA、RNA、タンパク質など)するだけのエネルギーを速やかに放出する。
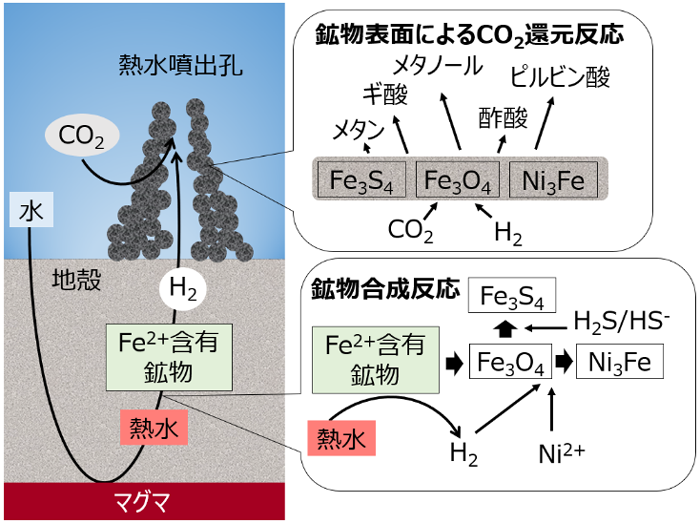
最初の数ステップで触媒となる酵素には、鉄とニッケルと硫黄からなる無機のクラスターが含まれている。このクラスターは、物理的に電子をCO2へ運び、反応性の高いアセチル基を生成する役割を担っている。このような無機のクラスターは、
- 基本的に鉱物(岩石)であり、熱水噴出孔に析出する鉄硫黄鉱物と構造が近い(図53)。
アルカリ熱水孔の地球化学的現象とメタン生成菌や酢酸生成菌による生化学的現象は極めて類似性が高いため、これらは単なる類似というより本質的な『相同性』(ある形態や遺伝子が共通の祖先に由来する性質)と見なすことが適切である。つまり、
- 「アルカリ熱水孔の地球化学的現象」が「メタン生成菌や酢酸生成菌による生化学的現象」を直接的に引き起こした
と推測することが妥当である。
しかし、アセチルCoAの提供する最大の利点は、
- 「炭素の代謝とエネルギーの代謝が交錯する場所」にその存在が見受けられることである(注47)。
アセチルCoAの、生命の起源との関連性については、ベルギーの著名な生化学者クリスティアン・ド・デューヴが、1990年代の初めに「アセチルCoAは有機合成を推進するだけでなく、リン酸と直接反応しアセチルリン酸を生成する」と明らかにしていた(図54)。
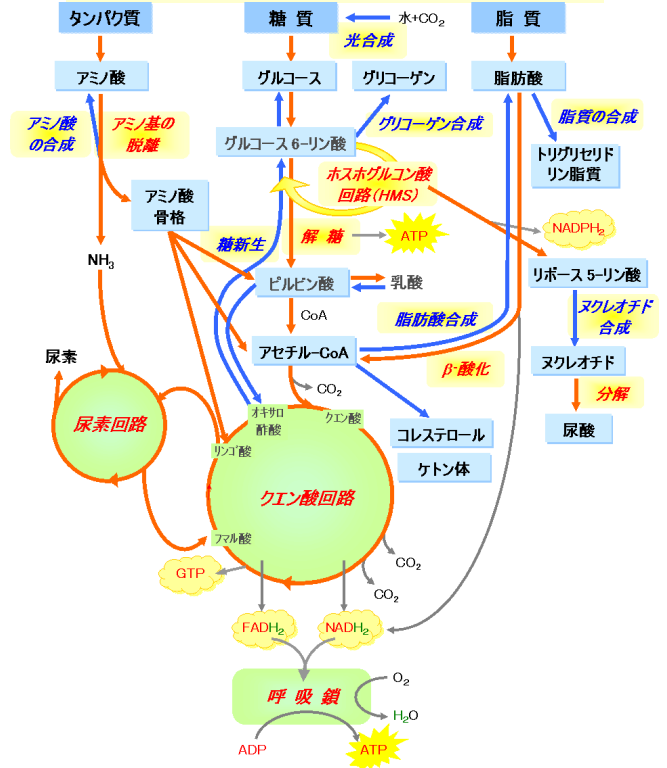
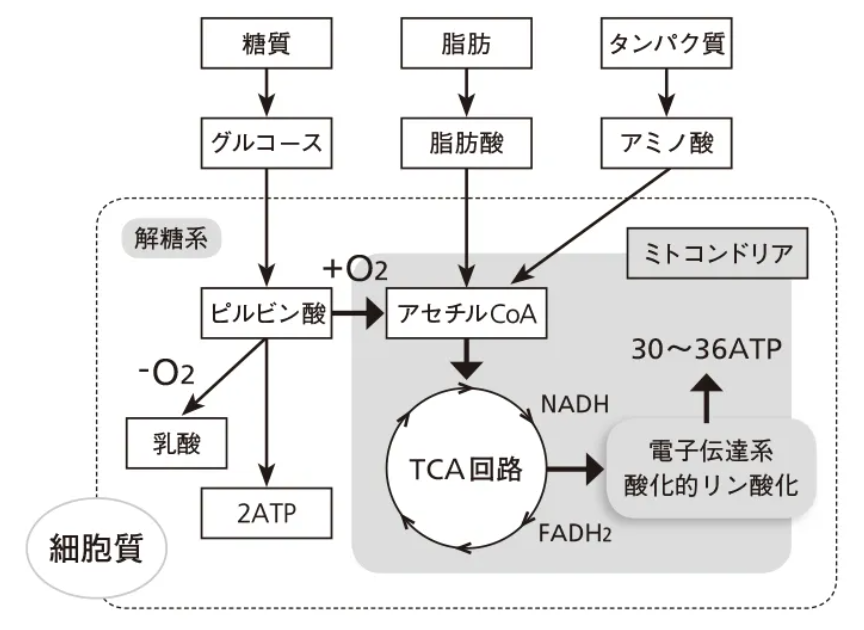
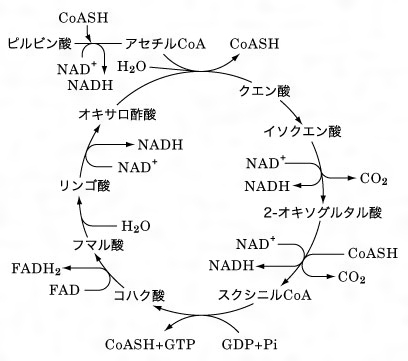
(注47)『代謝マップ』(図55)とそのエネルギー生成に注目した概要を図56に示す。炭素の代謝とエネルギーの代謝の交錯する場所に要となっているのが『アセチルCoA』であることがわかる。この図には『クエン酸回路』が示されているが、これは『トリカルボン酸tricarboxylic acid回路』とも呼ばれ、また短縮して『TCA回路』とも称される。これは呼吸の主要な代謝経路であり、動植物を通じて認識されているものである。酸素呼吸を行うほとんどの生物に普遍的に存在し、特に動植物や菌類ではミトコンドリアという細胞小器官の溶質部(ミトコンドリアマトリックス)に局在している。図57「クエン酸(TCA)回路」に示すように、TCA回路の最初の反応は、脂肪や炭水化物が代謝されて生成されたアセチルCoAとオキサロ酢酸が縮合してクエン酸を生成する反応である。クエン酸は回路を巡って再びオキサロ酢酸を生成する。図中の、CoASHは遊離の補酵素A、NAD=ニコチンアミドアデニンジヌクレオチド、NADH=還元型NAD、GTP=グアノシン三リン酸、GDP=グアノシン二リン酸、FAD=フラビンアデニンジヌクレオチド、Pi=リン酸、である。
この回路の主な役割は、電子伝達系(呼吸鎖)と協働し、酸素吸収を伴いながら炭水化物、脂肪、タンパク質を水と二酸化炭素に完全に分解し、生命活動に必要なエネルギー物質として重要な『ATP(アデノシン三リン酸)』を最も効率良く生成することにある。脂肪酸はミトコンドリアでの『β酸化』[*]により分解され、アセチルCoAを生ずる。糖は解糖によりピルビン酸を生じ、ピルビン酸はミトコンドリアに入ってCoAと反応してアセチルCoAを生じる。
[*]脂肪酸の代謝において脂肪酸を酸化して脂肪酸アセチルCoA(脂肪酸と補酵素Aのチオエステル)を生成し、そこからアセチルCoAを取り出す代謝経路のことである。β酸化は4つの反応の繰り返しから成り、反応が一順するごとにアセチルCoAが1分子生成され、最終生産物もアセチルCoAとなる。生成されたアセチルCoAはクエン酸回路に送られ、CO2へと酸化される。動物細胞では脂肪酸からエネルギーを取り出すための重要な代謝経路である。
合成されたATPは、ほとんどすべての生命現象、たとえば知覚、運動、成長、増殖などに広く利用される。
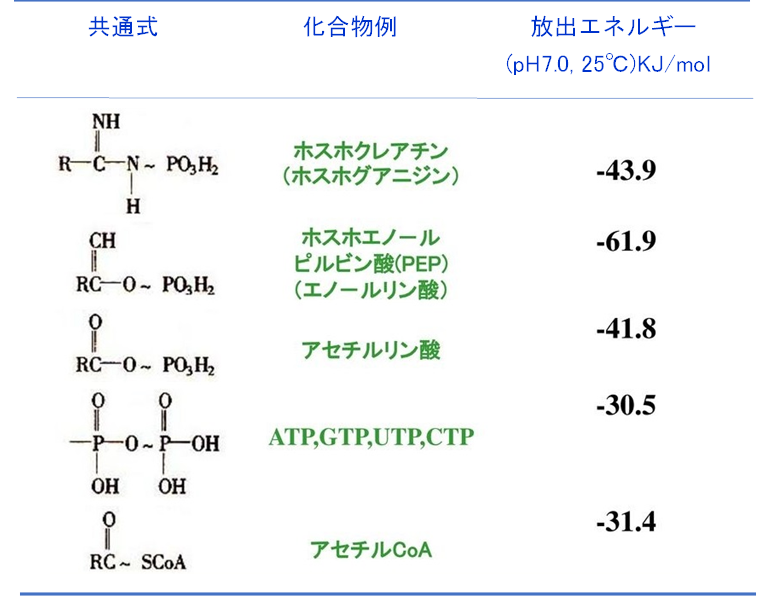
現代におけるATPと同等の重要性を持つエネルギー通貨ではないが、『アセチルリン酸』は現在も生命全般で広く用いられており、ATPと同様の機能を果たすことが可能である。高エネルギー化合物の例を図58に示すが、アセチルリン酸は著しく高いエネルギー放出を示す。
さらに、前節で述べたように、ATPは単にエネルギーを放出するだけでなく、
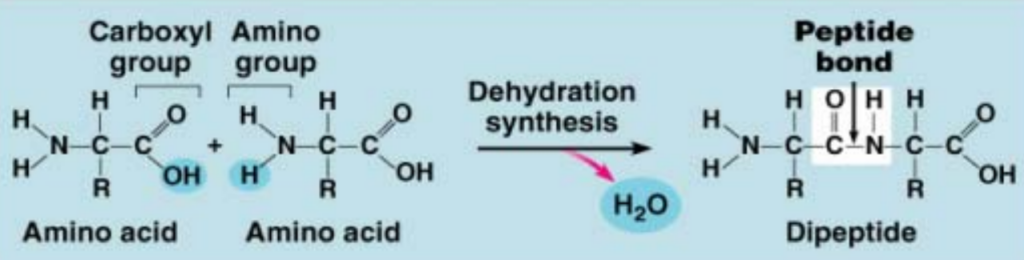
- 脱水反応を促進し、2個のアミノ酸などから水1分子を抽出して連鎖を形成する(図59)という作用を行う。
ニック・レーンらは実験室でこの現象を確認し、
- アセチルリン酸にも基本的に同等の化学反応が存在し、全く同じ機能を果たすことができることを明らかにした。
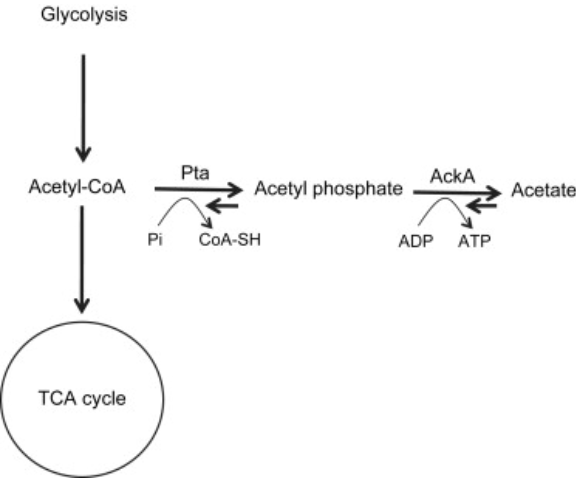
さらに、アセチルCoAからPta-AckA経路によりアセチルリン酸が形成される(図54)ため、
- 初期の炭素とエネルギーの代謝も、同じ単純なチオエステル、すなわちアセチルCoAによって促進されていた可能性がある。
しかし、アセチルCoAは、アセチル基が炭素2個の化合物であるとはいえ、CoAは複雑な分子である。そのため、アセチルCoAは明らかに自然選択の産物で、進化の過程において後から生成されたものである。したがって、アセチルCoA自体を前提とした議論は成り立たない。
一方で、アセチルCoAと同等の機能を果たし、更に単純な無生物の化合物が存在する。アセチルCoAの反応性は、『チオエステル結合』に由来する。この結合は硫黄原子に炭素が結びつき、その炭素に更に酸素が結びついたものにすぎない。化学式では次のように表される。
R―S―CO―CH3
ここで「R」は分子の「残り」の部分を指し、CoAである必要はない。CH3基ぐらい単純なものであってもよい。
- すると『チオ酢酸メチル』という低分子になる。
CH3―S―CO―CH3
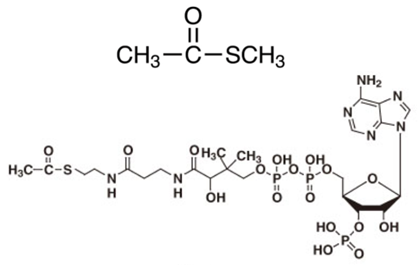
- 実は、この分子は反応性の高いチオエステルで、アセチルCoAと化学的に同等だが、その構造は単純で、アルカリ熱水噴出孔においてH2とCO2から生成することができる。実際に、クラウディア・フーバーとギュンター・ヴェヒターズホイザーは、COとCH3SHのみによってこの化合物を合成している。
さらに有用なことに、チオ酢酸メチルもアセチルCoAと同様に、リン酸と直接反応してアセチルリン酸を生成できる。
- したがって、この反応性の高いチオエステルは、新たな有機分子の合成を直接促進するだけでなく、アセチルリン酸を介してこれらの分子を重合し、タンパク質やRNAなどのより複雑な分子へと進化させる可能性がある。
実際に、ニック・レーンらの研究グループは、実験室で卓上型の反応装置を使用して、低濃度ではあるがアセチルリン酸を生成することに成功している。
まとめると、
アセチルCoA経路の原始的なバージョンは、理論上、アルカリ熱水噴出孔の微細孔内で原初の細胞が生まれるのに必要なすべての過程を推進することが可能であると考えられる。それは次の3つの段階を経る。
- 第一の段階では、触媒となる鉄硫黄鉱物を含む薄い無機の壁を介して、「プロトン勾配」が有機低分子の形成を促す(<物語り その4>図50)。これらの有機物は、前章で論じたとおり、「熱泳動」によって比較的低温の細孔内で濃縮され、優れた触媒の役割を果たす。これが生化学的メカニズム-分子間の相互作用と単純なポリマーの形成を促す反応前駆体の連続的な形成と濃縮-の起源である。
- 第二の段階では、熱水噴出孔の微細孔内で、単純な有機物から原始細胞が形成される。これは、有機物同士の物理的相互作用が自然にもたらす結果であり、物質の「自己組織化」現象によるものである。ただし、この過程によって形成された細胞状の散逸構造は、まだ遺伝的な基盤や本格的な複雑さを備えていない。
これらの単純な原始細胞は、有機合成を促進するプロトン勾配を利用すると考えられる。それは、熱水噴出孔自体の無機の壁ではなく、原始細胞自身の膜(例えば自然に形成される脂肪酸からの「脂質二重層」)を介したプロトン勾配である。このプロトン勾配を利用することで、複雑な分子の関与なしに[補注:タンパク質のような複雑な分子が関わる必要もなく]、先ほど触れた「チオ酢酸メチル」と「アセチルリン酸」の生成を促し、「炭素とエネルギーの両方の代謝」を促進することができると考えられる。
この段階には、最初の段階のものと比べてひとつ重要な違いがある。
- 新たな有機物が、今度は、原始細胞そのものの中で、有機の膜を挟んだ天然のプロトン勾配に促されて生成するのである。これは、受動的な化学反応ではなく、炭素、エネルギー、プロトンの継続的な流れによって強制的に促されたものなのである。
要は、こうした反応は、酸性になった金属の豊富な海へ水素の豊富な還元性のアルカリ流体が流れ込んで生じる不安定な非平衡から散逸構造をもたらす、ただ一つ起こりえる、熱力学的平衡に至る唯一の経路なのである。
- 第三の段階は、遺伝コードの誕生である。真正な遺伝性が発生し、原始細胞が自己のおおよそ正確なコピーを作成する能力を獲得する。
合成と分解の速度差に基づく初期の形態選択は、本格的な自然選択に取って代わり、遺伝子とタンパク質を持つ原始細胞の集団が熱水噴出孔の微細孔内で生存競争を始める。進化の標準的なメカニズムがついに初期の細胞に、リボソームやATP合成酵素など、現在でも生命体で広く保持されている高度なタンパク質を生成する能力を与えたのである。
そして、
細菌と古細菌の共通祖先であるLUCAが、アルカリ熱水噴出孔の細孔内に生息していたと考えられる。これにより、無生物からLUCAへ至るまでの三段階が全て、熱水孔の細孔内で生じたと考えることができる。それぞれの段階は、無機の壁や有機の膜を介して生成されるプロトン勾配によって促進される。しかし、ATP合成酵素などの高度なタンパク質の登場は、LUCAに至る困難な道のりの終盤のステップであった。
なお、原初の生化学的メカニズムの詳細について―遺伝コードの起源等の本質的で難解な問題―は、多くの研究者が研究を行っているものの、まだ解明されていない。
ここまで述べてきたのは、「生命の誕生を駆り立てた原動力は何だったのか?」という問いに対する、物理法則に基づく自然な考え方である。そして、遺伝子、タンパク質、LUCAの登場に至るまで、複雑な生体分子の形成を促した炭素、エネルギー、触媒がどこから生じたのかを示す上で、「理論上の難点は存在しない」と断言することができる。
また、熱水孔のシナリオは、図61で示されている「メタン生成菌-H2とCO2を起点としてアセチルCoA経路によって生きる古細菌-の生化学的メカニズム」に美しくつながっている。この古代の細胞と思われる生物は、膜を介してプロトン勾配を生み出し(図62、注48)[補注:H2とCO2の反応で生じるエネルギーが、細胞膜の外へプロトン(H+)を押し出す原動力となっている]、まさにアルカリ熱水噴出孔が提供しているものを生産している。
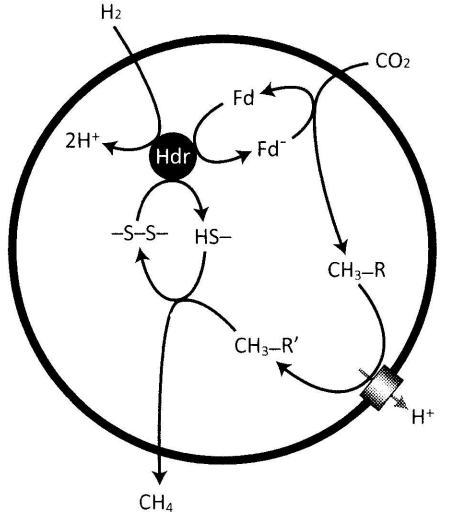
(注48)図中の『ヒドロゲナーゼ(Hdr)』という酵素が、「フェレドキシン(Fd)」と「ジスルフィド結合(-S-S-)」を同時に還元する触媒として働き、その過程でH2の電子を2個利用する。次にフェレドキシンがCO2を還元し、メチル基(-CH3)を生じ、これが補助因子Rと結合する。このメチル基はその後、第二の補助因子(R’)に移行し、その過程で、膜を超えて2個のH+を吸収するエネルギーが放出される。最後の段階では-CH3がHS-によって還元されてメタン(CH4)となる。全体的に、H2とCO2からメタン(CH4)を生成する過程で放出されるエネルギーの一部が、細胞膜を介してH+勾配に変換されるのである。
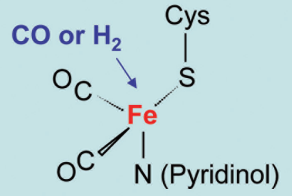
そのプロトン勾配は、膜に埋め込まれた鉄硫黄タンパク質-『エネルギー変換ヒドロゲナーゼ(energy-converting hydrogenase)、略してEch』(図63)-によってアセチルCoA経路の進行を促す(図64、注49)。
(注49)『エネルギー変換ヒドロゲナーゼ(Ech)』はフェレドキシン(Fd)を直接還元し、フェレドキシンがその後自身の電子をCO2に渡してメチル基(-CH3)を生成し、これがさらにCOと反応して代謝の要となる「アセチルCoA」を生成する。同様に、H+の流れはATP合成酵素によってATP合成を促し、これがエネルギーの代謝となる。なお、ヒドロゲナーゼには進化的に異なるFe型、Fe-Fe型、およびNi-Fe 型の3種類が知られており、Fe 型は古細菌に分類されるメタン菌のみに見られ、さらにFe-Fe型も偏性嫌気性細菌に存在が限定されるのに対し、Ni-Fe型はバクテリアに広く分布する。
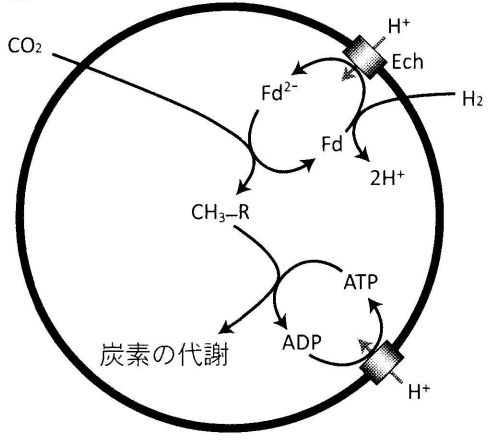
このタンパク質(Ech)は、膜を通じてプロトンをフェレドキシン(Fd)(注42)という別の鉄硫黄タンパク質へ送り込み、それが次にCO2を還元する。前章で、熱水孔内の薄いFeSの壁を隔てた天然のプロトン勾配が、H2とCO2の還元電位を変化させてCO2を還元することもありうると示唆した。これは、酵素Echがナノメートルスケールで行っていると考えられる。
- 酵素がタンパク質のわずか数オングストロームの隙間における厳密な物理的条件(プロトン濃度など)を制御することは一般的であり、Echがそれを行っている可能性がある。
- そうであるとすれば、初期の状態-短いポリペプチドが、脂肪酸で構成された原始細胞に組み込まれたFeS鉱物と結合することで安定化した状態-と現代の状態-遺伝子でコードされた膜タンパク質Echが、現代のメタン生成菌の炭素代謝を制御する状態-は、シームレスに接続されている可能性がある。
- いずれにせよ、現在、遺伝子とタンパク質の世界ではEchが、メタン生成によって生じるプロトン勾配を利用して、CO2の還元を促している。メタン生成菌はまた、プロトン勾配を利用して、ATP合成酵素によるATP合成を直接促進しているのである。
- したがって、炭素とエネルギーの代謝は、熱水孔が提供するプロトン勾配によって促進されるものと推測される。そして、最初期の原始細胞がアルカリ熱水孔に生息していたとすれば、彼らはこのプロトン勾配を利用して炭素とエネルギーの代謝を行っていた可能性があると考えられる。
以上の観点から、以下のまとめが可能である。
初期の地球の環境が生命の誕生をどのように支援したかという観点から、研究を進めると、
- 定常的な炭素とエネルギーの流れと鉱物の触媒、天然の区画化が組み合わさった『アルカリ熱水噴出孔』が重要な環境であったと結論づけられる。
- しかしながら、この段階では、炭素とエネルギーの流れがH2とCO2の形をとるが、これら二つの素材が容易に反応しない、という問題が存在していた。
- そこで、熱水孔の細孔内に存在する薄い半導体の障壁を介した地球化学的な『プロトン勾配』が、反応のエネルギー障壁を克服する可能性があることを見出した。
- 『チオ酢酸メチル』(アセチルCoAと同等の機能)などの反応性の高いチオエステルを生成することで、プロトン勾配は炭素とエネルギーの代謝を助長し、熱水孔の細孔内に有機分子の蓄積をもたらす。『脱水反応』を容易にし、DNAやRNA、タンパク質などの複雑なポリマーの生成を可能にする。
- 遺伝コードがどのように生じたかといった説明は一旦置いておき、理論的に遺伝子とタンパク質を持つ原始的な細胞を生成したという観念的な議論を進めた結果、アルカリ熱水孔の細孔に生息し、天然のプロトン勾配に依存していた単純な細胞の集団が自然選択により進化し、細菌と古細菌の最後の『共通祖先LUCA』が生じた可能性を示すことができる。リボソームやEch、ATP合成酵素などの高度なタンパク質が自然選択により誕生し、それらは現在も保存されている。
地球であろうと、宇宙のどこかであろうと、最も現実的に生命を生成しうる環境は『アルカリ熱水噴出孔』であると考えられる。熱水孔は細胞に天然の『プロトン勾配』を利用させ、最終的には『細胞』自体を生み出す。その流れからすると、地球上のすべての細胞が『化学浸透共役』(注25:細胞内で、ATPの化学合成と、電子伝達系のエネルギーを利用したプロトンの膜輸送(浸透)が組になってエネルギー変換を行う機構)を利用していることは全く驚くべきことではない。そして、全宇宙の細胞も同様に「化学浸透共役」を利用することが予想される。
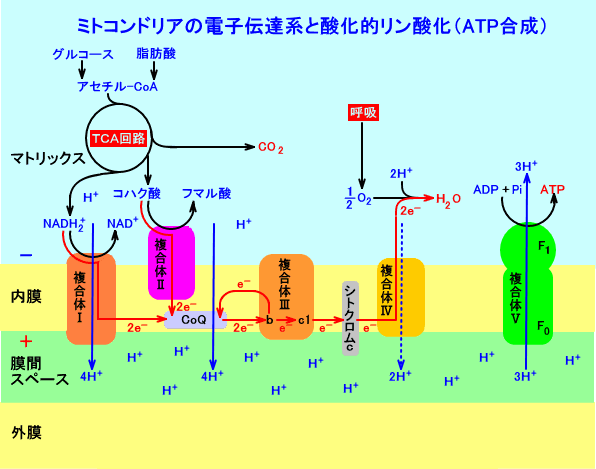
なお、プロトン勾配を積極的に利用している一連の『呼吸鎖』すなわち、ミトコンドリアの『電子伝達系』と『酸化的リン酸化(ATP合成)』を模式的に<物語り その3>に図33として示したが、参考として以下に再掲する。
図表
図51 アセチルCoAの構造式
株式会社コレット(https://www.colette-p.com/)
フスボンのサイト
(https://www.fusubon.com/what-is-ketone-bodies/)
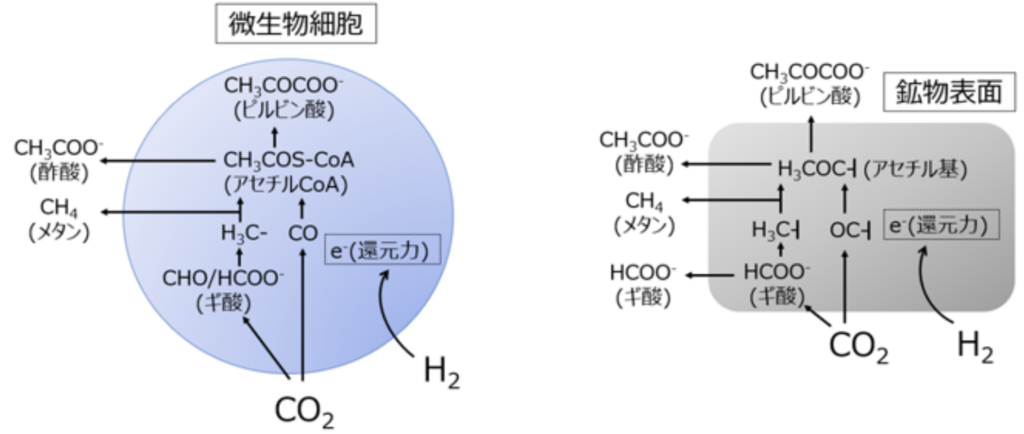
図52 メタン生成菌・酢酸生成菌が行っている還元的アセチルCoA経路
産総研マガジン、研究成果記事一覧2020年「生命のもととなる可能性のある有機物の合成反応を
実証」
(https://www.aist.go.jp/aist_j/press_release/pr2020/pr20200303_2/pr20200303_2.html)
図53 熱水噴出孔で作られる3種類の天然鉱物とそれらが触媒となる有機物合成反応
産総研マガジン、研究成果記事一覧2020年「生命のもととなる可能性のある有機物の合成反応を
実証」
(https://www.aist.go.jp/aist_j/press_release/pr2020/pr20200303_2/pr20200303_2.html)
図54 Pta(ホスホトランスアセチラーゼ)-AckA(酢酸キナーゼA)経路
Itzhak Mizrahi, Dvora Biran and Eliora Z. Ron,”Involvement of the Pta-AckA pathway in
protein folding and aggregation” Research in Microbiology 160 (2009) 80-84.
(https://www.sciencedirect.com/science/article/abs/pii/S0923250808001770)
図55 代謝マップ
地球資源論研究室・地球科学一般・生物資源・代謝
(http://earthresources.sakura.ne.jp/er/ES_R_S.html#anchor78612)
図56 エネルギー産生代謝マップの概要
医療法人社団 恵み野内科循環器クリニック、ドクターズブログ・糖質制限とケトン体の効用・第
58回 糖質制限とケトン体 がん治療
(https://megumino-clinic.com/648.html)
図57 クエン酸(TCA)回路
コトバンク、日本大百科全書(ニッポニカ)「TCA回路」
(https://kotobank.jp/word/TCA%E5%9B%9E%E8%B7%AF-100069)
図58 高エネルギー化合物
SlidePlayer(https://www.slideshare.net/)「生体酸化 Biological Oxidation」
(https://slidesplayer.net/slide/11400832/)
図59 2個のアミノ酸の脱水反応の例(ペプチド生成)
ADDISON WESLEY LONGMAN,INC.
(https://opencorporates.com/companies/us_ma/041016235)
図60 チオ酢酸メチル(上)とアセチルCoA(下)
コトバンク、栄養・生化学辞典「アセチルCoA」の解説
(https://kotobank.jp/word/%E3%82%A2%E3%82%BB%E3%83%81%E3%83%ABCoA-670121)
図61 原始的な微生物がもつ代謝と鉱物によるCO2還元反応の類似性
産総研マガジン、研究成果記事一覧2020年「生命のもととなる可能性のある有機物の合成反応を
実証」
(https://www.aist.go.jp/aist_j/press_release/pr2020/pr20200303_2/pr20200303_2.html)
図62 メタンの生成によるエネルギーの産出
「生命、エネルギー、進化THE VITAL QUESTION Why Is Life the Way It Is?」
ニック・レーン Nick Lane著、斉藤隆央訳、株式会社 みすず書房、2016年9月13日 第1刷、
2018年3月9日 第10刷
図18「メタンの生成によってエネルギーを生み出す.A」、161頁
図63 鉄型ヒドロゲナーゼの構造
嶋 盛吾(マックスプランク陸生微生物学研究所):「[Fe]-ヒドロゲナーゼ(Hmd)の構造解
析から見えてきたヒドロゲナーゼ活性中心の収斂進化」、生化学 第80巻 第9号 846
(https://www.jbsoc.or.jp/seika/wp-content/uploads/2013/11/80-09-08.pdf)
図64 エネルギー変換ヒドロゲナーゼEchによるアセチルCoA経路の促進
「生命、エネルギー、進化THE VITAL QUESTION Why Is Life the Way It Is?」
ニック・レーン Nick Lane著、斉藤隆央訳、株式会社 みすず書房、2016年9月13日 第1刷、
2018年3月9日 第10刷
図18「メタンの生成によってエネルギーを生み出す.B」、161頁

